¿Qué es el sulforafano?
Sulforafano es un fitoquímico, una sustancia dentro del grupo isotiocianato de compuestos organosulfurados, que se encuentra en los vegetales crucíferos, como el brócoli, la col, la coliflor y las coles de Bruselas. También se puede encontrar en bok choy, col rizada, coles, hojas de mostaza y berros. Los estudios de investigación han demostrado que el sulforafano puede ayudar a prevenir varios tipos de cáncer Activando la producción de Nrf2., o factor relacionado con el factor eritroide 2 nuclear, un factor de transcripción que regula los mecanismos antioxidantes protectores que controlan la respuesta de la célula a los oxidantes. El propósito del siguiente artículo es describir la función del sulforafano.
Índice del contenido
Resumen
El sistema antioxidante KEAP1-Nrf2-ARE es un medio principal por el cual las células responden al estrés oxidativo y xenobiótico. El sulforafano (SFN), un isotiocianato electrofílico derivado de vegetales crucíferos, activa la vía KEAP1-Nrf2-ARE y se ha convertido en una molécula de interés en el tratamiento de enfermedades en las que el estrés oxidativo crónico desempeña un papel etiológico importante. Aquí demostramos que las mitocondrias de las células epiteliales pigmentadas de la retina humana (RPE-1) tratadas con SFN se someten a una hiperfusión que es independiente tanto de Nrf2 como de su inhibidor citoplasmático KEAP1. Se ha informado que la fusión mitocondrial es citoprotectora al inhibir la formación de poros en las mitocondrias durante la apoptosis, y de manera consistente, mostramos la citoprotección independiente de Nrf2 de células tratadas con SFN expuestas al inductor de apoptosis, estaurosporina. Mecánicamente, el SFN mitiga el reclutamiento y / o la retención del factor de fisión soluble Drp1 en las mitocondrias y en los peroxisomas, pero no afecta la abundancia general de Drp1. Estos datos demuestran que las propiedades beneficiosas de SFN se extienden más allá de la activación del sistema KEAP1-Nrf2-ARE y requieren una mayor interrogación dado el uso actual de este agente en múltiples ensayos clínicos.
Palabras clave: Sulforafano, Nrf2, Drp1, Mitocondrias, Fisión, Fusión, Apoptosis
Introducción
Sulforaphane es un inhibidor independiente de Nrf2 de la fisión mitocondrial
El sulforafano (SFN) es un compuesto de isotiocianato derivado de la dieta más comúnmente de los vegetales crucíferos [56]. Se genera en las plantas como una respuesta xenobiótica a la depredación a través de la liberación vesicular de la enzima hidrolítica miosinasa de las células dañadas; esta enzima convierte los glucosinolatos en isotiocyantes [42]. Durante las últimas dos décadas, el SFN se ha caracterizado ampliamente por sus propiedades anticancerígenas, antioxidantes y antimicrobianas [57]. Gran parte de esta eficacia se ha atribuido a la capacidad de SFN para modular la vía de señalización del elemento de respuesta antioxidante (ARE) KEAP1-Nrf2, aunque se han identificado actividades adicionales del compuesto, incluida la inhibición de la actividad de la histona desacetilasa y la progresión del ciclo celular [ 29]. Nrf2 es el principal factor de transcripción antioxidante y, en condiciones de homeostasis, su estabilidad se suprime a través de la acción del complejo citoplasmático de la ligasa Cullin3KEAP1 [20]. Específicamente, Nrf2 se recluta a la ligasa Cullin3KEAP1 mediante la unión al adaptador de sustrato dimérico KEAP1 y posteriormente se modifica con cadenas poliUb que apuntan al factor de transcripción para la degradación mediada por proteasoma. Esta rotación constitutiva limita la vida media de Nrf2 en celdas sin estrés a ~ 15 min [30], [33], [46], [55]. En respuesta a numerosos tipos de estrés, principalmente el estrés oxidativo, KEAP1, una proteína rica en cisteína, actúa como un sensor redox, y la modificación oxidativa de cisteínas críticas, particularmente C151, de KEAP1NUMX disocia Nrf2-KEAP1 de CUL3XXXXXXXXXXXXXNXX-KEAP2® 8], [20], [55]. En particular, SFN, y posiblemente otros activadores Nrf2, imitan el estrés oxidativo modificando C151 de KEAP1, por ejemplo, [21]. La estabilización de Nrf2 permite su translocación al núcleo donde induce la expresión de una batería de genes de desintoxicación y antioxidantes de fase II. Nrf2 se une a los elementos promotores de la respuesta antioxidante (ARE) de sus genes diana relacionados mediante la heterodimerización con pequeñas proteínas Maf [19]. Este sistema presenta una respuesta dinámica y sensible a los antioxidantes indirectos como SFN, los radicales libres generados por las mitocondrias [16] u otras fuentes fisiológicas de estrés oxidativo [41].
Las mitocondrias son orgánulos subcelulares dinámicos que regulan una gran cantidad de funciones celulares que van desde la producción de ATP y el amortiguamiento de calcio intracelular hasta la regulación redox y la apoptosis [13], [49]. Las mitocondrias también representan la principal fuente de especies reactivas de oxígeno (ROS) dentro de la célula. Por lo tanto, es necesaria una regulación adecuada de la función mitocondrial para optimizar la producción de ATP para satisfacer las necesidades celulares al tiempo que minimiza los efectos potencialmente dañinos de la producción excesiva de radicales libres. Un requisito crítico para la modulación fina de la función mitocondrial es la capacidad de las mitocondrias para funcionar de manera independiente como máquinas bioquímicas y como parte de una red amplia y receptiva.
La morfología y la función de la red mitocondrial están determinadas por un equilibrio regulado entre la fisión y la fusión. La fisión mitocondrial es necesaria para la herencia de las mitocondrias de células hijas durante la división celular [28], así como para la degradación autofágica y selectiva de las mitocondrias despolarizadas o dañadas, denominada mitofagia [1]. A la inversa, se requiere la fusión para complementar los genomas mitocondriales y compartir componentes de la cadena de transporte de electrones entre las mitocondrias vecinas [54]. A nivel molecular, la fisión mitocondrial y la fusión están reguladas por grandes GTPasas similares a dinaminas. Tres enzimas regulan principalmente la fusión: las mitofusinas 1 y 2 (Mfn1 / 2) son proteínas de membrana externa de dos pases que median la fusión de la membrana externa mediante interacciones heterotípicas entre mitocondrias adyacentes [15], [25], [37], mientras que OPA1 es un interior Proteína de membrana que asegura simultáneamente la conectividad de la matriz regulando la fusión de las membranas internas [5]. La actividad GTPasa de las tres proteínas se requiere para una fusión robusta [5], [18], y OPA1 está más regulada por la proteólisis compleja dentro de la membrana interna mitocondrial por las proteasas OMA1 [14], PARL [6], y YME1L [45] ]. Es importante destacar que se requiere un potencial de membrana mitocondrial intacto para una fusión eficiente con el fin de suprimir la integración de las mitocondrias dañadas y sanas [26].
La fisión mitocondrial es principalmente catalizada por una proteína citosólica llamada proteína relacionada con Dynamin 1 (Drp1 / DNM1L). Drp1 se contrata desde el citosol hasta sitios prospectivos de fisión en la membrana externa mitocondrial [43]. Los principales receptores para Drp1 en la membrana externa son el factor de fisión mitocondrial (Mff) [32] y, en menor medida, la Fisión 1 (Fis1) [51]. Además, se descubrió un receptor señuelo, MIEF1 / MiD51, que actúa para limitar aún más la actividad de la proteína Drp1 en los posibles sitios de fisión [58]. Una vez acoplado a la membrana externa mitocondrial, Drp1 se oligomeriza en estructuras en forma de espiral alrededor del cuerpo de la mitocondria y luego utiliza la energía derivada de la hidrólisis de GTP para mediar la escisión física de las membranas internas y externas mitocondriales [17]. Los túbulos derivados del retículo endoplásmico actúan como un constrictor inicial de las mitocondrias antes de la oligomerización Drp1, lo que subraya la revelación de que las mitocondrias no constrictas son más anchas que la circunferencia permisiva de una espiral Drp1 completa [12]. La dinámica de la actina también es importante para las interacciones ER-mitocondrias que preceden a la fisión mitocondrial [24]. Además de su papel en la fisión mitocondrial, Drp1 cataliza la fisión de los peroxisomas [40].
Drp1 es muy similar a la proteína dinamina bien caracterizada porque ambas proteínas contienen un dominio GTPasa N-terminal, un dominio Medio que es crítico para la autooligomerización, y un dominio efector de GTPasa C-terminal [31]. Drp1 logra una selectividad para las membranas mitocondriales a través de una combinación de interacciones con sus proteínas receptoras Mff y Fis1 y también a través de su afinidad por la cardiolipina fosfolípida específica de mitocondrias a través del dominio único de inserción B de Drp1 [2]. Drp1 generalmente existe como un homotetramer en el citoplasma, y el ensamblaje de orden superior en los sitios de fisión mitocondrial está mediado por el dominio Medio de Drp1 [3].
Dado el vínculo implícito entre la función mitocondrial y la ruta KEAP1-Nrf2-ARE, investigamos los efectos de la activación de Nrf2 en la estructura y función mitocondrial. Aquí demostramos que SFN induce hiperfusión mitocondrial que, inesperadamente, es independiente tanto de Nrf2 como de KEAP1. Este efecto de SFN es a través de una inhibición de la función Drp1. También demostramos que SFN confiere resistencia a la apoptosis que es independiente de Nrf2 e imita a la observada en células agotadas de Drp1. Estos datos indican colectivamente que, además de estabilizar y activar Nrf2, SFN modula la dinámica mitocondrial y preserva la capacidad y la supervivencia celular.
Resultados
Sulforaphane Induce Hiperfusión Independiente De Nrf2 / KEAP1 De Mitocondria
En el curso del estudio de los efectos de la activación de Nrf2 en la dinámica de la red mitocondrial, descubrimos que el tratamiento de células epiteliales del pigmento retinal humano inmortalizadas (RPE-1) con sulforafano (SFN), un potente activador de la señalización de Nrf2, indujo una fusión robusta de La red mitocondrial en comparación con las células de control tratadas con vehículo (Fig. 1A y B). La morfología de las mitocondrias en estas células se parecía mucho a la de las mitocondrias en las células agotadas por ARNsi de Drp1 endógeno, el principal factor de fisión mitocondrial (Fig. 1A). Este resultado planteó la intrigante idea de que la fisión mitocondrial y el estado de fusión responden directamente a los niveles de Nrf2 en la célula. Sin embargo, la estimulación de células con otros estabilizadores y activadores de Nrf2, como el inhibidor del proteasoma MG132, el pro-oxidante tBHQ, o la desactivación del inhibidor de Nrf2 KEAP1 no indujo fusión mitocondrial (Fig. 1A y B). La estabilización de Nrf2 mediante estas manipulaciones se confirmó mediante transferencia de Western para Nrf2 endógeno (Fig. 1C). Además, la expresión de Nrf2 era prescindible para la fusión mitocondrial inducida por SFN, ya que la eliminación de Nrf2 endógeno con siRNA no pudo contrarrestar este fenotipo (Fig. 1D-F). Debido a que SFN estimula la vía KEAP1-Nrf2-ARE modificando de manera covalente los residuos de cisteína de KEAP1 [21], eliminamos KEAP1 para determinar si la hiperfusión mitocondrial inducida por SFN es de carácter independiente, pero no está obsesionada con el contenido, no está obsesionada con la presencia de NN. Sin embargo, el agotamiento de KEAP1 tampoco logró anular la fusión mitocondrial inducida por SFN (Fig. 2G-I). De hecho, SFN invirtió la morfología de pro-fisión inducida por el agotamiento de KEAP1 (Fig. 1G, panel b versus panel d). Estos resultados indican que el tratamiento con SFN causa una fusión mitocondrial independiente de la vía canónica KEAP1-Nrf1-ARE y nos llevó a interrogar si la SFN afecta directamente a los componentes de la maquinaria de fusión o fisión mitocondrial.
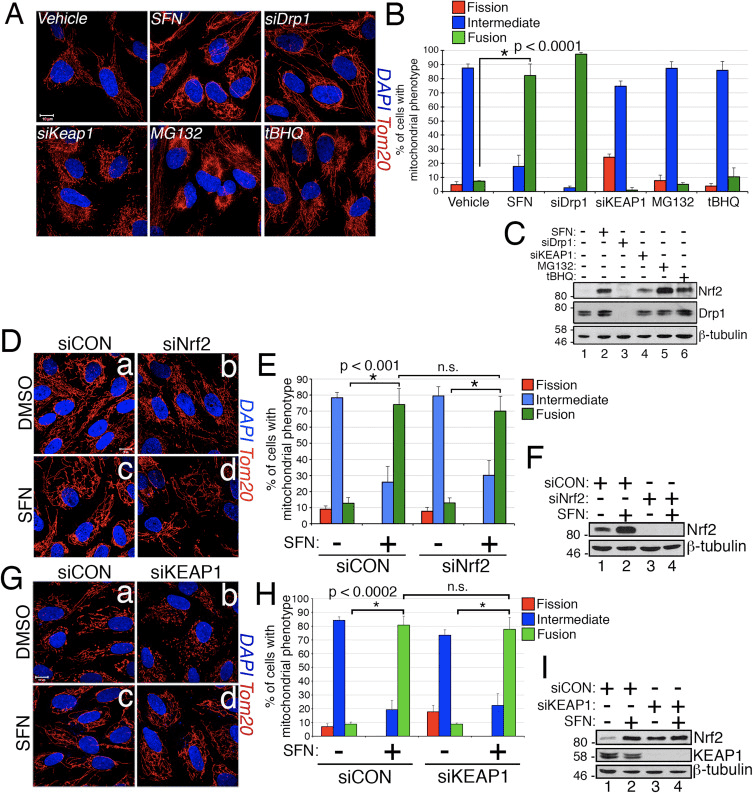
Sulforaphane daña la asociación mitocondrial de Drp1
En base al hallazgo de que el tratamiento con SFN induce hiperfusión mitocondrial, razonamos que este fenotipo era una consecuencia de una actividad de fusión excesiva o una inhibición de la actividad de fisión. Para discriminar entre estas dos posibilidades, comparamos la morfología de los peroxisomas en presencia y ausencia de SFN. Los peroxisomas son similares a las mitocondrias, ya que son orgánulos dinámicos cuya forma y longitud están constantemente en flujo [44]. Los peroxisomas contienen tanto Fis1 como Mff en su membrana externa y, como consecuencia, son objetivos para la fisión mediada por Drp1 [22], [23]. Sin embargo, los peroxisomas no utilizan la maquinaria de fusión de la red mitocondrial y, en consecuencia, no se someten a fusión [39]. Más bien, la fisión peroxisomal se opone al alargamiento de los peroxisomas existentes mediante la adición de novo de membranas y proteínas [44]. Debido a que los peroxisomas carecen de Mfn1 / 2 y OPA1, razonamos que si SFN activa la maquinaria de fusión en lugar de inhibir la maquinaria de fisión, la longitud del peroxisoma no se vería afectada. En las células tratadas con vehículo, los peroxisomas se mantienen como orgánulos puntiformes cortos y redondos (Fig. 2, paneles byd). Sin embargo, el tratamiento con SFN aumentó la longitud del peroxisoma en ~ 2-fold en comparación con las células de control (Fig. 2, paneles f y h). Además, muchos de los peroxisomas se pellizcaron cerca del centro, lo que indica un posible defecto de escisión (Fig. 2, panel h, puntas de flecha). Del mismo modo, los peroxisomas en las células transfectadas con Drp1 siRNA fueron anormalmente largos (Fig. 2, paneles j y l), lo que confirma que Drp1 es necesario para la fisión peroxisomal y sugiere que el tratamiento con SFN causa fenotipos mitocondriales y peroxisómicos al interrumpir la maquinaria de la fisión.
A continuación, determinamos cómo SFN restringe la función Drp1. Las posibilidades incluían reducciones en los niveles de expresión, reclutamiento / retención en las mitocondrias, oligomerización o actividad enzimática de la GTPasa. Un déficit en cualquiera de estos podría resultar en una reducción de la fisión mitocondrial y la hiperfusión. No detectamos cambios reproducibles en los niveles de proteína Drp1 después del tratamiento con SFN (Figs. 1C y 3A
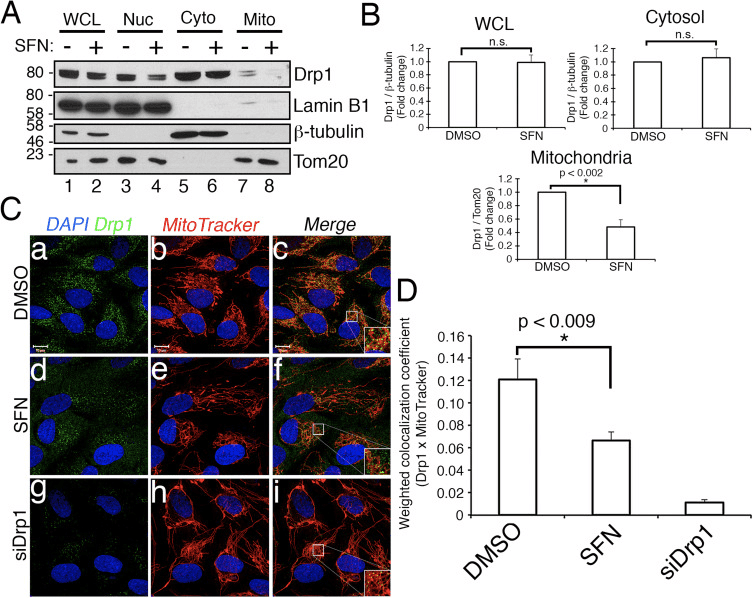
Sulforaphane confiere protección contra la apoptosis inducida por estaurosportina independiente de Nrf2
Trabajos anteriores han demostrado que la fisión mitocondrial es permisiva en la formación de poros en la membrana mitocondrial externa generada por Bax / Bak durante la apoptosis [11]. Se ha demostrado que Drp1 se ha reclutado selectivamente para mitocondrias durante la apoptosis [11] y, en concordancia con esto, se han observado mitocondrias fragmentadas al principio del proceso [27]. A la inversa, se cree que la inhibición de la fisión mitocondrial inhibe la apoptosis al bloquear la formación de los poros de la membrana externa que permiten la liberación del citocromo c [53]. En consecuencia, la estimulación de la fusión mitocondrial retrasa la progresión de la apoptosis inducida por compuestos que incluyen estaurosporina (STS) [14]. Para determinar si SFN protege a las células RPE-1 de la apoptosis mediada por STS y, en caso afirmativo, si esto requiere Nrf2, establecimos un ensayo para inducir fácilmente la escisión de poli ADP ribosa polimerasa (PARP), un sustrato de caspasa activada-3 y
Discusión
Hemos descubierto que SFN modula la dinámica de fusión / fisión mitocondrial independientemente de sus efectos en la ruta KEAP1-Nrf2-ARE. Esto es intrigante debido a un vínculo asumido entre la disfunción mitocondrial y la producción de ROS y la necesidad de sofocar los radicales libres derivados de la mitocondria a través de la activación de Nrf2. Este impacto funcional adicional de SFN es de importancia potencial dado que hay más de 30 ensayos clínicos actualmente en curso que prueban SFN para el tratamiento de una variedad de enfermedades que incluyen cáncer de próstata, enfermedad pulmonar obstructiva y enfermedad de células falciformes [7], [10], [ 47].
Debido a que SFN es un isotiocianato [56] y activa la señalización de Nrf2 al acilar directamente las cisteínas críticas de KEAP1 para suprimir la degradación de Nrf2 [21], se deduce que SFN ejerce sus efectos pro-fusión modulando la actividad de una fisión o un factor de fusión a través de una modificación de cisteína. . Nuestros datos respaldan firmemente que Drp1 sea regulado negativamente por SFN, aunque aún no se ha determinado si la GTPasa es un objetivo directo de la acilación. A pesar de esta brecha de conocimiento, la función de Drp1 está siendo claramente comprometida por SFN a medida que tanto las mitocondrias como los peroxisomas se vuelven
Materiales y methods
Ensayos de apoptosis
Las células se sembraron y transfectaron con ARNip como se indica a continuación. Las células se pretrataron con sulforafano 50 \ mu M durante 2 h para inducir la fusión mitocondrial y luego se trataron con estaurosporina 1 \ mu M para inducir la apoptosis. En el momento de la recolección, el medio se recogió en tubos individuales y se sometió a centrifugación a alta velocidad para sedimentar las células apoptóticas. Este sedimento celular se combinó con células adherentes y se solubilizó en tampón Laemmli concentrado 2 veces. Las muestras se sometieron a inmunotransferencia de tipo anti-PARP.
Generación de construcciones CRISPR / Cas9
Para crear LentiCRISPR / eCas9 1.1, LentiCRISPR v2 (addgene #52961) primero se cortó con Age1 y BamH1. A continuación, se amplificó la PCR con los voladizos de la fuente de luz de la mano de la máquina de la mano y de la mano de la mano de la máquina de la mano, y también de la mano de la mano. Las secuencias de sgRNA se determinaron utilizando Benchling.com. Los parámetros se establecieron para apuntar a la secuencia de codificación con las puntuaciones más altas dentro del objetivo y más bajas fuera del objetivo. Las siguientes secuencias (secuencia de dirección subrayado, HS sgNFE9L9 # 1.1 sentido CACCGCGACGGAAAGAGTATGAGC, antisentido AAACGCTCATACTCTTTCCGTCGC; hs sgNFE71814L1 # 1 CACCGGTTTCTGACTGGATGTGCT sentido, AAACAGCACATCCAGTCAGAAACC antisentido; hs sgNFE2L2 # 1 sentido CACCGGAGTAGTTGGCAGATCCAC, antisentido AAACGTGGATCTGCCAACTACTCC) se reasociaron y se ligaron en BsmB2 cortó LentiCRISPR / eCas2 2. Se seleccionaron células RPE-2 infectadas con lentitis con puromicina y se mantuvieron como una población agrupada. El golpe de gracia se confirmó mediante inmunofluorescencia y transferencia de Western.
Cultivo Celular y Transfecciones
Se cultivaron células epiteliales de pigmento de la retina humana transformadas con telomerasa (RPE-1) (ATCC) en Medio Águila Modificada de Dulbecco (DMEM) que contiene 1 g / L de glucosa suplementada con penicilina, estreptomicina, cóctel de aminoácidos no esencial de 1X (Life Technologies), y 10% de suero bovino fetal (Life Technologies). Para las transfecciones de ARNip, se sembraron células 30,000-35,000 / ml durante la noche. Las células recibieron ARNsi nNMX nM diluido en DMEM sin suero y se combinaron con reactivo de transfección con interferón 10 (PolyPlus). Para la sensibilización a la apoptosis, las células recibieron ARNsi 0.3 nM Bcl-XL. Las células se recogieron 1-2 días después de la transfección.
Productos químicos, anticuerpos y oligos siRNA
Anticuerpos contra? -Tubulina (señalización celular),? -Tubulina (Sigma), Drp1 (BD Biosciences), KEAP1 (Proteintech), Lamin B1 (Abcam), PARP (señalización celular), PMP70 (Abcam) y Tom20 (BD Biosciences) ) se utilizaron en diluciones 1: 1000 para transferencia Western y para inmunofluorescencia. En casa, se utilizó anticuerpo de conejo anti-Nrf2 a 1: 2000 para la transferencia de Western [34], [59]. Se utilizaron sulforafano (Sigma) y estaurosporina (Tocris) a 50 \ mu M y 1 \ mu M respectivamente. Se usaron ARNip contra Drp1 (Dharmacon), Nrf2 (Dharmacon), KEAP1 (Señalización celular) y Bcl-XL (Señalización celular) a 10 nM a menos que se indique lo contrario.
Inmunofluorescencia y etiquetado in vivo.
Las células sembradas en cubreobjetos de vidrio de 18 mm se trataron con vehículo o fármaco, se fijaron en formaldehído al 3.7% y luego se permeabilizaron en Triton X-0.2 / PBS al 100% en hielo durante 10 min. Los anticuerpos primarios se incubaron en albúmina de suero bovino (BSA) al 3% en PBS durante la noche a 4ºC. Después de los lavados con PBS, las células se incubaron durante 1 h en anticuerpos secundarios conjugados, Alexa488 o Alexa546, apropiados para la especie (diluidos 1: 1000) y DAPI (Sigma) 0.1 μg / ml en BSA / PBS al 3%. Las mitocondrias se visualizaron mediante inmunofluorescencia anti-Tom20 o incubando células en 200 nM MitoTracker Red CMXRos (Molecular Probes, Inc.) en DMEM sin suero durante 30 min a 37ºC antes de la fijación.
Microscopía y Análisis de Imagen.
Las muestras de inmunofluorescencia se vieron en un microscopio confocal LSM710 (Carl Zeiss). Las micrografías se capturaron utilizando objetivos de inmersión en aceite 63X o 100X e imágenes ajustadas y mejoradas utilizando Adobe Photoshop CS6. El análisis de co-localización se realizó utilizando la función de co-localización de Carl Zeiss LSM710 con umbrales establecidos manualmente mientras se desconoce la identidad de las muestras. Las barras de escala en todo, a menos que se indique lo contrario, son 10 µm. La morfología mitocondrial se evaluó mediante puntuación ciega. Si las mitocondrias de una célula se mantenían como múltiples puntos redondos, discriminados, la célula se calificaba como "fisión". Si las mitocondrias individuales eran indistinguibles y toda la red mitocondrial aparecía continua, la célula se calificaba como "fusión". Todas las demás células, incluidas aquellas con mitocondrias agrupadas, se calificaron como "intermedias".
Fraccionamientos subcelulares
Las células RPE-1 se cultivaron hasta la confluencia. Después de un lavado con PBS, las células se sometieron a centrifugación a 600 xg durante 10 min y se resuspendieron en 600 μl de tampón de aislamiento (manitol 210 mM, sacarosa 70 mM, MOPS 5 mM, EDTA 1 mM pH 7.4 + PMSF 1 mM). La suspensión se lisó 30 veces en un homogeneizador Dounce. Una fracción del homogeneizado se conservó como un "lisado de células completas". El resto se sometió a centrifugación a 800 xg durante 10 min para sedimentar los núcleos. Los sobrenadantes se sometieron a centrifugación a 1500 xg durante 10 min para limpiar los núcleos restantes y las células no lisadas. Este sobrenadante se sometió a centrifugación a 15,000 xg durante 15 min para sedimentar las mitocondrias. El sobrenadante se conservó como la "fracción citosólica". El sedimento se lavó suavemente con PBS y se resuspendió en tampón de aislamiento. La concentración de proteína de cada fracción se midió mediante un ensayo de ácido bicinconínico (BCA) y las cantidades equivalentes de proteína se resolvieron mediante SDS-PAGE.
Western Blot
Las células se lavaron en PBS y se solubilizaron en 2 veces el tampón de solubilización Laemmli concentrado (100 mM Tris [pH 6.8], 2% SDS, 0.008% bromofenol azul, 2% 2-mercaptoetanol, 26.3% glicerol y 0.001

El sulforafano es un producto químico de la colección de isotiocianatos de sustancias organosulfuradas obtenidas de vegetales crucíferos, como el brócoli, el repollo, la coliflor, la col rizada y las coles, entre otros. El sulforafano se produce cuando la enzima mirosinasa transforma la glucorafanina, un glucosinolato, en sulforafano, también conocido como sulforafano-glucosinolato. Los brotes de brócoli y la coliflor tienen la mayor concentración de glucorafanina o el precursor de sulforafano. Los estudios de investigación han demostrado que el sulforafano mejora las capacidades antioxidantes del cuerpo humano para prevenir diversos problemas de salud.
Dr. Alex Jimenez DC, CCST Insight
El sulforafano y sus efectos sobre el cáncer, la mortalidad, el envejecimiento, el cerebro y el comportamiento, las enfermedades cardíacas y más
Los isotiocianatos son algunos de los compuestos vegetales más importantes que puede obtener en su dieta. En esto
Secciones clave:
- 00: 01: 14 - Cáncer y mortalidad
- 00: 19: 04 - Envejecimiento
- 00: 26: 30 - Cerebro y comportamiento
- 00: 38: 06 - Resumen final
- 00: 40: 27 - Dosis
Línea de tiempo completa:
- 00: 00: 34 - Introducción de sulforafano, un enfoque importante del video.
- 00: 01: 14 - Consumo de vegetales crucíferos y reducciones en la mortalidad por todas las causas.
- 00: 02: 12 - Riesgo de cáncer de próstata.
- 00: 02: 23 - Riesgo de cáncer de vejiga.
- 00: 02: 34 - El cáncer de pulmón en riesgo de los fumadores.
- 00: 02: 48 - Riesgo de cáncer de mama.
- 00: 03: 13 - Hipotético: ¿qué sucede si ya tiene cáncer? (intervencionista)
- 00:03:35 - Mecanismo de conducción plausible
el cancer y datos asociativos de mortalidad. - 00: 04: 38 - Sulforafano y cáncer.
- 00:05:32 - Evidencia animal que muestra
fuerte Efecto del extracto de brote brócoli en el desarrollo de tumores de vejiga en ratas. - 00: 06: 06 - Efecto de la suplementación directa de sulforafano en pacientes con cáncer de próstata.
- 00: 07: 09 - Bioacumulación de metabolitos de isotiocianato en el tejido mamario real.
- 00: 08: 32 - Inhibición de las células madre del cáncer de mama.
- 00: 08: 53 - Lección de historia: Brassicas se establecieron con propiedades de salud incluso en la antigua Roma.
- 00: 09: 16 - Capacidad de sulforafano para mejorar la excreción de carcinógenos (benceno, acroleína).
- 00: 09: 51 - NRF2 como un interruptor genético a través de elementos de respuesta antioxidante.
- 00: 10: 10: cómo la activación de NRF2 mejora la excreción de carcinógenos a través de los conjugados de glutatión-S.
- 00: 10: 34 - Las coles de Bruselas aumentan la glutatión-S-transferasa y reducen el daño al ADN.
- 00: 11: 20 - La bebida de brotes de brócoli aumenta la excreción de benceno en un 61%.
- 00: 13: 31 - El homogeneizado de brotes de brócoli aumenta las enzimas antioxidantes en las vías respiratorias superiores.
- 00: 15: 45 - Consumo de vegetales crucíferos y mortalidad por enfermedades del corazón.
- 00: 16: 55 - El brote en polvo de brócoli mejora los lípidos en la sangre y el riesgo general de enfermedad cardíaca en los diabéticos tipo 2.
- 00:19:04 - Comienzo de
envejecimiento . - 00:19:21 - La dieta enriquecida con sulforafano mejora
esperanza de vida de escarabajos de 15 a 30% (en ciertas condiciones). - 00: 20: 34 - Importancia de la inflamación baja para la longevidad.
- 00: 22: 05 - Las verduras crucíferas y el brote de brócoli en polvo parecen reducir una amplia variedad de marcadores inflamatorios en los humanos.
- 00: 23: 40 - Resumen del medio video: cáncer, envejecimiento, secciones
- 00: 24: 14: los estudios con ratones sugieren que el sulforafano podría mejorar la función inmunológica adaptativa en la vejez.
- 00:25:18 - El sulforafano mejoró el crecimiento del cabello en un modelo de ratón con calvicie.
Imagen en 00: 26: 10. - 00: 26: 30 - Inicio del cerebro y sección de comportamiento.
- 00: 27: 18 - Efecto del extracto de brotes de brócoli en el autismo.
- 00: 27: 48 - Efecto de la glucorafanina sobre la esquizofrenia.
- 00: 28: 17 - Inicio de la discusión sobre la depresión (mecanismo plausible y estudios).
- 00:31:21 - Un estudio con ratones utilizando 10 modelos diferentes de depresión inducida por estrés muestra que el sulforafano es igualmente efectivo como la fluoxetina (
prozac ). - 00: 32: 00 - El estudio muestra que la ingesta directa de glucorafanina en ratones es igualmente efectiva para prevenir la depresión por el modelo de estrés por derrota social.
- 00: 33: 01 - Inicio de la sección de neurodegeneración.
- 00: 33: 30 - Sulforafano y enfermedad de Alzheimer.
- 00: 33: 44 - Sulforaphane y enfermedad de Parkinson.
- 00: 33: 51 - Sulforaphane y la enfermedad de Hungtington.
- 00: 34: 13 - Sulforaphane aumenta las proteínas de choque térmico.
- 00: 34: 43 - Inicio de la sección de lesión cerebral traumática.
- 00: 35: 01 - Sulforaphane inyectado inmediatamente después de un TBI mejora la memoria (estudio en ratones).
- 00: 35: 55 - Sulforafano y plasticidad neuronal.
- 00:36:32 - El sulforafano mejora el aprendizaje en
modelo de la diabetes tipo II en ratones. - 00:37:19 - Sulforafano y
duchenne distrofia muscular. - 00: 37: 44 - Inhibición de la miostatina en células satélite de músculo (in vitro).
- 00: 38: 06 - Resumen de video tardío: mortalidad y cáncer, daño en el ADN, estrés oxidativo e inflamación, excreción de benceno, enfermedad cardiovascular, diabetes tipo II, efectos en el cerebro (depresión, autismo, esquizofrenia, neurodegeneración), NRF2.
- 00: 40: 27 - Reflexiones sobre cómo calcular una dosis de brotes de brócoli o sulforafano.
- 00: 41: 01 - Anécdotas sobre la brotación en el hogar.
- 00: 43: 14 - En temperaturas de cocción y actividad de sulforafano.
- 00: 43: 45 - Conversión de las bacterias intestinales del sulforafano a partir de glucorafanina.
- 00: 44: 24 - Los suplementos funcionan mejor cuando se combinan con la mirosinasa activa de vegetales.
- 00: 44: 56 - Técnicas de cocción y verduras crucíferas.
- 00: 46: 06 - Isotiocianatos como goitrógenos.
Agradecimientos
Sciencedirect.com/science/article/pii/S2213231716302750
¿Cómo se produce el sulforafano?
El calentamiento disminuye la actividad de la proteína epitiospecificadora y aumenta la formación de sulforafano en el brócoli
Resumen
El sulforafano, un isotiocianato del brócoli, es uno de los anticarcinógenos derivados de los alimentos más potentes. Este compuesto no está presente en la verdura intacta, sino que se forma a partir de su precursor de glucosinolato, glucorafanina, por la acción de la mirosinasa, una enzima tioglucosidasa, cuando se tritura o se mastica el tejido de brócoli. Sin embargo, varios estudios han demostrado que el rendimiento de sulforafano a partir de la glucorafanina es
El precalentamiento de los brotes de brócoli y los brotes a 60 ° C aumentó significativamente la formación de sulforafano (SF) catalizada por la mirosinasa en extractos de tejidos vegetales después de la trituración. Esto se asoció con disminuciones en la formación de nitrilo de sulforafano (Nitrilo SF) y en la actividad de la proteína epitioespecificante (ESP).
Palabras clave: Brócoli, Brassica oleracea, Crucíferas, Cáncer, Anticarcinógeno, Sulforafano, Nilforforano, Nitrilo, Proteína Epitioespecífica, Quinona Reductasa
En conclusión, el sulforafano es un fitoquímico encontrado en
Comisariada por el Dr. Alex Jiménez
Remitido desde: Sciencedirect.com

Tema adicional de discusión: Dolor de espalda agudo
El dolor de espalda es una de las causas más frecuentes de discapacidad y días perdidos en el trabajo en todo el mundo. El dolor de espalda se atribuye a la segunda razón más común para las visitas al consultorio del médico, superado en número solo por las infecciones de las vías respiratorias superiores. Aproximadamente el 80% de la población experimentará dolor de espalda al menos una vez a lo largo de su vida. La columna vertebral es una estructura compleja compuesta de huesos, articulaciones, ligamentos y músculos, entre otros tejidos blandos. Debido a esto, lesiones y / o condiciones agravadas, como hernias discales, eventualmente puede conducir a síntomas de dolor de espalda. Las lesiones deportivas o las lesiones por accidentes automovilísticos suelen ser la causa más frecuente de dolor de espalda; sin embargo, a veces los movimientos más simples pueden tener resultados dolorosos. Afortunadamente, las opciones de tratamiento alternativo, como la atención quiropráctica, pueden ayudar a aliviar el dolor de espalda mediante el uso de ajustes espinales y manipulaciones manuales, mejorando finalmente el alivio del dolor.

EXTRA EXTRA | TEMA IMPORTANTE: ¿Quiropráctico recomendado en El Paso, TX?
***
Publicar descargo de responsabilidad *
Alcance de la práctica profesional *
La información aquí contenida en "¿Qué es el sulforafano?" no pretende reemplazar una relación personal con un profesional de la salud calificado o un médico con licencia y no es un consejo médico. Lo alentamos a que tome decisiones de atención médica basadas en su investigación y asociación con un profesional de la salud calificado.
Información del blog y debates sobre el alcance
Nuestro alcance informativo se limita a la quiropráctica, musculoesquelética, medicina física, bienestar, contribuyendo etiológico alteraciones viscerosomáticas dentro de las presentaciones clínicas, la dinámica clínica del reflejo somatovisceral asociado, los complejos de subluxación, los problemas de salud delicados y/o los artículos, temas y debates de medicina funcional.
Brindamos y presentamos colaboración clínica con especialistas de diversas disciplinas. Cada especialista se rige por su ámbito de práctica profesional y su jurisdicción de licencia. Utilizamos protocolos funcionales de salud y bienestar para tratar y apoyar la atención de lesiones o trastornos del sistema musculoesquelético.
Nuestros videos, publicaciones, temas, asuntos e ideas cubren cuestiones clínicas, problemas y temas que se relacionan y respaldan directa o indirectamente nuestro ámbito de práctica clínica.*
Nuestra oficina ha intentado razonablemente proporcionar citas de apoyo y ha identificado el estudio o los estudios de investigación relevantes que respaldan nuestras publicaciones. Proporcionamos copias de los estudios de investigación de respaldo disponibles para las juntas reguladoras y el público a pedido.
Entendemos que cubrimos asuntos que requieren una explicación adicional de cómo puede ayudar en un plan de atención o protocolo de tratamiento en particular; por lo tanto, para discutir más a fondo el tema anterior, no dude en preguntar Dr. Alex Jiménez, DC, o póngase en contacto con nosotros en 915-850-0900.
Estamos aquí para ayudarlo a usted y a su familia.
Bendiciones
El Dr. Alex Jimenez corriente continua MSACP, enfermero*, CCCT, IFMCP*, CIFM*, ATN*
email: coach@elpasomedicinafuncional.com
Licenciado como Doctor en Quiropráctica (DC) en Texas & New Mexico*
Número de licencia de Texas DC TX5807, Nuevo México DC Número de licencia NM-DC2182
Licenciada como Enfermera Registrada (RN*) en Florida
Licencia de Florida N.° de licencia de RN RN9617241 (Control No. 3558029)
Estado compacto: Licencia multiestatal: Autorizado para ejercer en 40 Estados*
Matriculado actualmente: ICHS: MSN* FNP (Programa de enfermera practicante familiar)
Dr. Alex Jiménez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Mi tarjeta de presentación digital




